mRNA(信使核糖核酸)是分子生物学中心法则中的关键分子。近年来,以mRNA疫苗为代表的mRNA递送技术在生物医学的前沿领域迅速扩展,尤其是在预防或治疗蛋白质表达异常相关疾病方面展现出巨大潜力。然而,mRNA的易被降解特性使其需要递送系统来保护其进入目标细胞。此外,mRNA的非肝器官(如肺、脾脏等)靶向递送仍面临较大挑战。因此,开发新的具有不同器官靶向mRNA递送性能的载体材料,对拓宽mRNA疗法的应用范围具有重要意义。



图1 IAJD及其与mRNA共组装形成DNP示意图
基于单组分可离子化两亲性Janus树枝状大分子(IAJD)的mRNA递送系统因其良好的稳定性和高效的递送效率而崭露头角。IAJD是一种新型的mRNA递送载体,由亲水和疏水枝状结构组成,利用一步“注射”的自组装方法将其与mRNA共组装可以得到封装mRNA的树枝状大分子囊泡纳米颗粒(dendrimersome nanoparticle, DNP)。近日,研究团队聚焦IAJD这一新型mRNA递送平台,在Angewandte Chemie International Edition发表题为One-Component Ionizable Amphiphilic Janus Dendrimers for Targeted mRNA Delivery的minireview,系统综述了IAJD的设计、合成、mRNA递送以及器官靶向递送性能。文章的第一作者是实验室博士研究生朱鹏宇。
不同的IAJD分子能够高效地将mRNA递送到肝脏,以及肺、脾脏和淋巴结等多个器官,为治疗特定器官疾病mRNA药物的研发提供了新的思路。例如,脾脏和淋巴结是人体重要的免疫器官,它们在免疫细胞的激活和免疫反应的发生中起着关键作用。将mRNA 递送到脾脏和淋巴结,可以激活免疫系统产生特异性的免疫反应,这对于开发新型疫苗和免疫疗法具有重要意义。一系列的IAJD分子均表现出脾脏和淋巴结优先靶向的性质(图2)。通过对分子结构分析和体内递送效应优化发现,不对称的偶数/偶数疏水链配对表现出更加特异的脾脏靶向递送性质,而在对称的对应结构中则观察到肝脏和脾脏均有分布的现象。然而,这种脾脏靶向递送的潜在机制仍未明确。
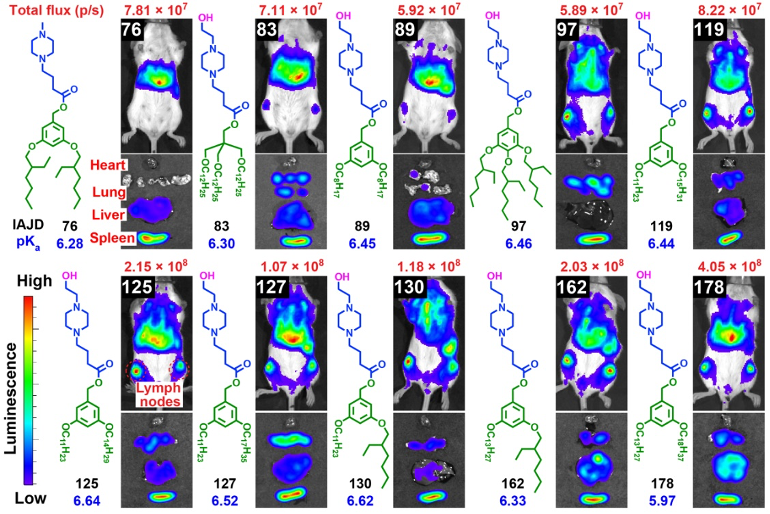
图2 代表性脾脏和淋巴结靶向IAJDs及其小鼠体内递送荧光素酶mRNA效果
肺是人体呼吸系统的核心器官,对于肺部疾病的治疗,如急性肺损伤、肺癌等,将mRNA精准递送到肺部组织以实现局部的蛋白表达,是一种有很有希望的治疗策略。许多IAJD分子展现出了优异的肺部靶向递送效果(图3),其中IAJD34在小鼠体内递送萤火虫荧光素酶mRNA至肺部后,表达出的荧光强度达到了1.5*108 p/s。最近已经有将IAJD34用于TGF-β mRNA肺部靶向递送的研究,证明了基于IAJD的肺靶向mRNA递送系统在治疗急性肺损伤等肺部疾病方面的巨大潜力。
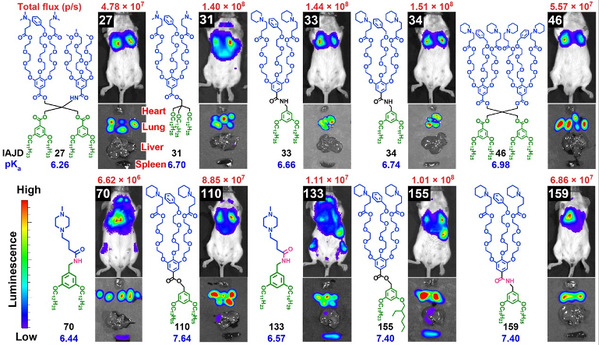
图3 代表性肺部靶向IAJDs及其小鼠体内递送荧光素酶mRNA效果
这篇minireview系统总结了IAJD载体在器官靶向mRNA递送领域的研究进展,并讨论了IAJD结构与器官靶向递送效果的构效关系。需要说明的是,IAJD作为一类新型树状大分子基mRNA递送平台,与成熟的脂质纳米颗粒(LNP)递送系统相比,仍处于初步研究阶段,但已显现出优异的应用潜力。本工作通过系统总结关于IAJD以及代表性的树状大分子mRNA递送载体的近期研究进展,重点阐述IAJD的器官靶向mRNA递送特性及其构效关系,旨在为开发更加高效的mRNA递送平台和新一代mRNA纳米药物提供启发和指引。
论文信息:
One-Component Ionizable Amphiphilic Janus Dendrimers for Targeted mRNA Delivery
Pengyu Zhu, Yongsheng Li*, Dapeng Zhang*
Angewandte Chemie International Edition. DOI: 10.1002/anie.202505304
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202505304